Cáncer de Cabeza y Cuello
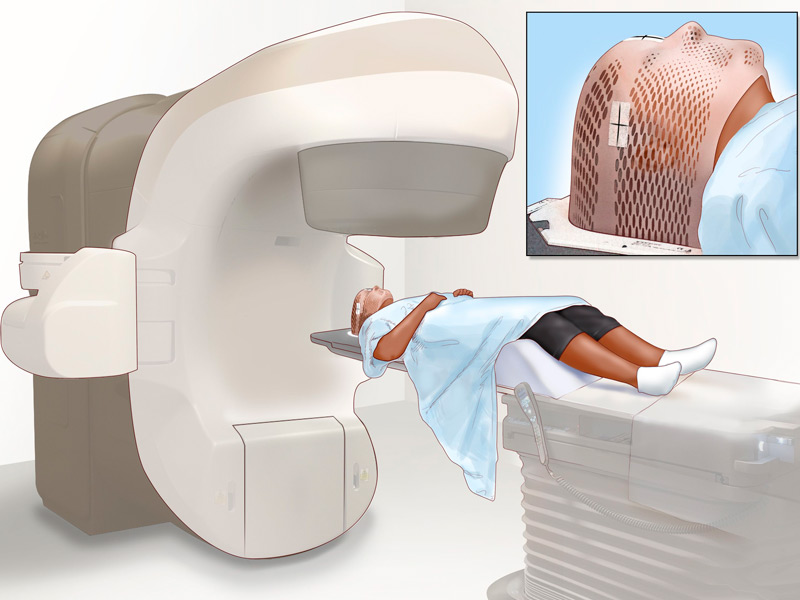
¿Qué es el cáncer de cabeza y cuello?
Los cánceres de cabeza y cuello, generalmente, comienzan en las células escamosas que revisten las superficies húmedas y mucosas del interior de la cabeza y del cuello (por ejemplo, dentro de la boca, de la nariz y de la garganta). El cáncer de células escamosas se llama, con frecuencia, carcinoma de células escamosas de cabeza y cuello. Los cánceres de cabeza y cuello se categorizan, a su vez, de acuerdo a la zona de la cabeza o del cuello en la que empiezan. Estas zonas son: Cavidad oral, Faringe, Laringe, Senos paranasales, cavidad nasal y, Glándulas salivales. Los cánceres de cerebro, ojo, esófago, glándula tiroides así como los de cuero cabelludo, de piel, de huesos y músculos de la cabeza y cuello no se clasifican generalmente como cáncer de cabeza y cuello.
A continuación, el detalle de algunas de estos tratamientos:
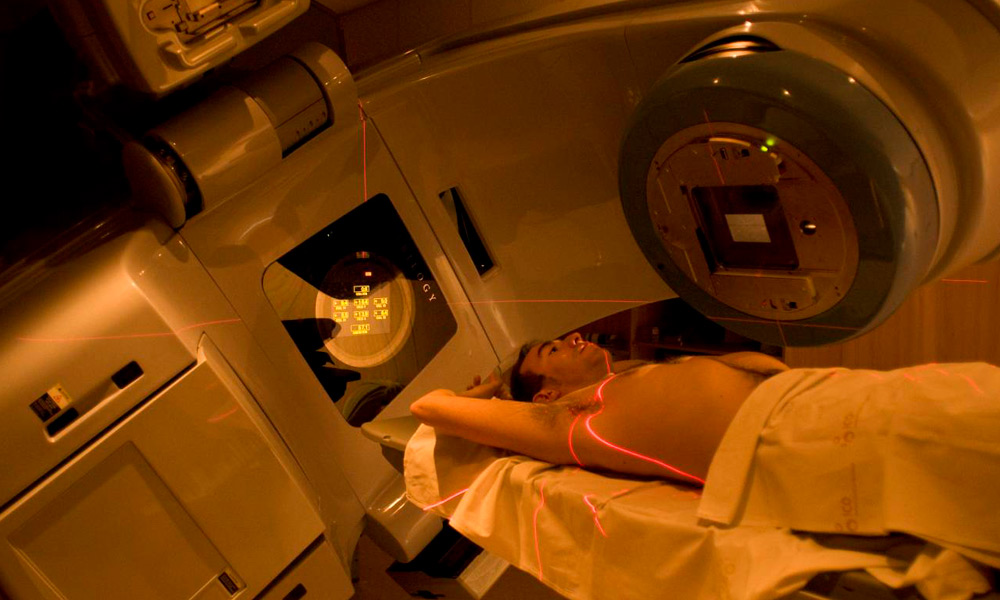
RADIOTERAPIA EN 4D: Sincroniza el tratamiento con la respiración del paciente. Esta novedosa técnica de radioterapia beneficia a pacientes con lesiones en tumores móviles al considerar desde el momento de la planificación del tratamiento el ciclo respiratorio del paciente.
Para ello el sistema de adquisición de imágenes del paciente, no solo toma las imágenes en un instante determinado, sino que se obtienen una serie de imágenes con la zona de tratamiento en las distintas posiciones que puede adoptar. En el sistema de planificación estas imágenes se pueden representar reproduciendo el movimiento real, considerando la respiración del paciente.
Esta técnica se emplea en lesiones en las que la zona tratar tiene mucha movilidad involuntaria.
En el Centro Médico de Radioterapia Siglo XXI tenemos amplia experiencia en la aplicación de última tecnología para el tratamiento de lesiones con radioterapia. Mediante la utilización de IMRT o Radioterapia de Intensidad modulada los pacientes reciben altas dosis de tratamiento de forma milimétricamente precisa, esto se traduce en una significativa disminución en la cantidad de tejido sano que es sometido a dosis de radiación, menos efectos secundarios, mejor preservación del tejido sano y una mayor optimización del tiempo de tratamiento del paciente (menos días de tratamiento que con radioterapia convencional).
Sumado a esto, con la nueva tecnología de radioterapia en 4D los ciclos respiratorios del paciente son considerados en la planificación del tratamiento. De esta forma el equipo y dosis se calibrarán para aplicar las dosis de tratamiento en las fases más óptimas del ciclo respiratorio, aumentando la efectividad y precisión del tratamiento de aquellos tumores o lesiones móviles.
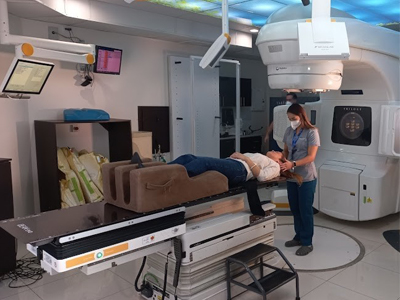
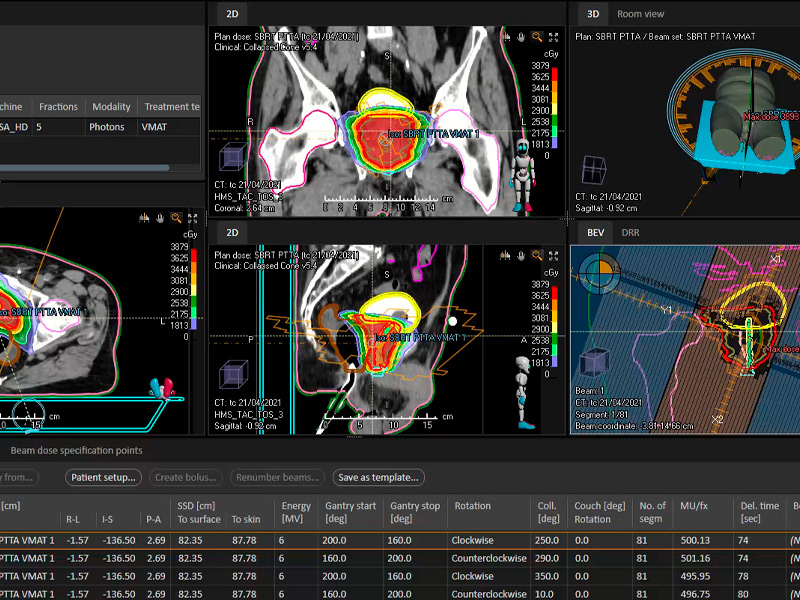
RADIOTERAPIA GUIADA POR IMÁGENES (IGRT): La Radioterapia con Imágenes guiadas o IGRT combina imágenes de tomografías computarizadas con radioterapia durante cada sesión de tratamiento. Esto permite determinar de la forma más precisa posible el área a tratar y proteger al máximo las áreas circuncidantes a la zona de tratamiento.
Esta tecnología lo que hace es ubicar al paciente en el punto exacto para irradiar casi de forma exclusiva la lesión y no dañar órganos importantes; tomando en cuenta variables milimétricas. Esta tecnología no está disponible en sistemas de radioterapia convencionales.
RADIOTERAPIA DE INTENSIDAD MODULADA (IMRT): La Radioterapia de Intensidad Modulada o IMRT es una tecnología a través de un sistema computarizado permite administrar dosis de radiación precisas a un tumor o a áreas específicas dentro de un tumor y reducir las dosis en tejidos sanos.
Esta tecnología combinada con las ventajas de nuestro acelerador lineal ofrecen la llamada Arco Terapia, que es la capacidad de irradiar una lesión desde 360 diferentes ángulos, garantizando la más alta calidad en el tratamiento en un tiempo sumamente corto (aproximadamente 3 minutos). De esta manera se aumenta la comodidad del paciente y los niveles de precisión del mismo.
RADIOCIRUGÍA: Altas dosis en pocos tratamientos (1-5 sesiones). La Radiocirugía o SBRT se utiliza en el tratamiento de tumores de tamaño pequeño a mediano.
A pesar de su nombre y en comparación con la radioterapia tradicional, es un procedimiento no quirúrgico que entrega radiación sumamente enfocada en dosis mucho más altas y en solamente uno o pocos tratamientos. Este tratamiento es posible gracias al desarrollo de tecnologías de radiación altamente avanzadas que permiten la entrega de dosis máximas dentro del blanco, mientras se reducen al máximo la dosis que recibe le tejido sano circundante. El objetivo es administrar dosis que destruyan el tumor y logren un máximo control local.